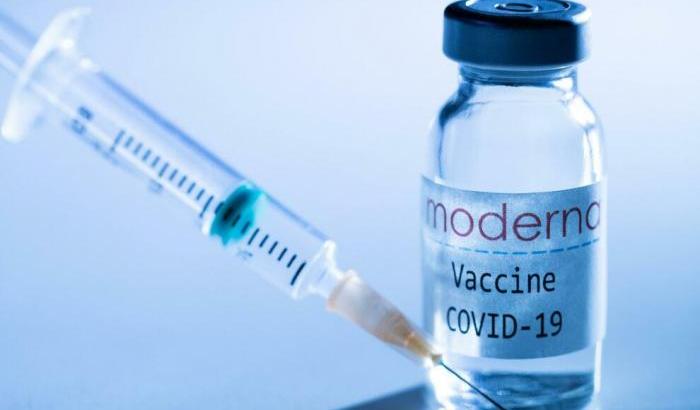
L’Agenzia Europea del Farmaco (Ema) ha accellerato sul vaccino di Moderna: “Nelle ultime settimane, l’Ema ha compiuto buoni progressi nella valutazione della domanda di autorizzazione all’immissione in commercio per il vaccino mRna-1273 contro Covid-19 di Moderna. Un dialogo continuo con l’azienda ha fatto sì che le domande sorte durante la valutazione fossero prontamente seguite e affrontate dall’azienda”.
Tenuto debito conto dei progressi compiuti il team di esperti ha fissato per il 6 gennaio 2021 una riunione straordinaria per concludere, se possibile, la propria valutazione. La riunione prevista per il 12 gennaio 2021 “verrà mantenuta se necessario”.
Oggi, “prima del previsto”, Moderna “ha presentato l’ultimo pacchetto di dati in sospeso necessario per la valutazione della domanda. Contiene informazioni specifiche per la produzione del vaccino per il mercato dell’Ue”, precisa l’Ema. “Siamo stati in grado di rivedere i calendari per la valutazione dei vaccini Covid-19 grazie agli incredibili sforzi di tutti coloro che sono coinvolti in queste valutazioni: i presidenti dei comitati scientifici, i relatori e le loro squadre di valutazione, esperti scientifici in tutti i membri dell’Ue Stati Uniti e il mio staff all’Ema”, ha affermato Emer Cooke, direttore esecutivo dell’Ema, che ha anche sottolineato che questi timing, come per qualsiasi medicinale, sono stabiliti in via provvisoria.
Una volta che il Comitato di esperti raccomanda l’autorizzazione all’immissione in commercio, la Commissione europea accelererà il processo decisionale per concedere il via libera valido in tutti gli Stati membri entro pochi giorni. L’autorizzazione all’immissione in commercio garantisce che i vaccini Covid-19 soddisfino “gli stessi elevati standard Ue di tutti i vaccini e medicinali”. Il via libera “sarà valido in tutti gli Stati membri dell’Ue contemporaneamente, consentendo a tutti i Paesi di avviare contemporaneamente le loro campagne di vaccinazione”. La valutazione scientifica sui vaccini anti-Covid “sarà indipendente – sottolinea l’Ema – e guidata dalle esigenze di salute pubblica e dei pazienti. La raccomandazione si baserà sulla forza delle prove scientifiche su sicurezza, qualità ed efficacia di un vaccino e nient’altro”.
L'Agenzia Europea del farmaco accelera sul vaccino di Moderna: valutazione entro il 6 gennaio
Tenuto debito conto dei progressi compiuti il team di esperti ha fissato per il 6 gennaio 2021 una riunione straordinaria per concludere, se possibile, la propria valutazione.

Preroll
globalist Modifica articolo
17 Dicembre 2020 - 18.02
ATF
Native
Articoli correlati
Salute / La Vitamina D ha effetti sull'umore